3,5-Dinitro-4-chlorbenzotrifluorid
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
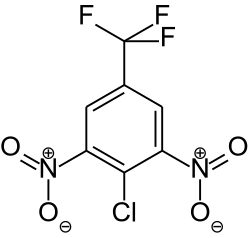
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 3,5-Dinitro-4-chlorbenzotrifluorid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C7H2ClF3N2O4 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 270,55 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
3,5-Dinitro-4-chlorbenzotrifluorid (Chloralin) ist eine chemische Verbindung aus der Gruppe der Chlorbenzotrifluoride.
Gewinnung und Darstellung
3,5-Dinitro-4-chlorbenzotrifluorid kann durch eine Reaktion von p-Chlortoluol mit Fluorwasserstoff zu p-Chlorbenzotrifluorid und anschließender Reaktion mit Salpetersäure und Schwefelsäure gewonnen werden. Alternativ kann auch die Carboxygruppe der 3,5-Dinitro-4-chlorbenzoesäure mit Schwefeltetrafluorid durch Trifluorid ersetzt werden.[3]
Verwendung
3,5-Dinitro-4-chlorbenzotrifluorid ist ein Zwischenprodukt für die Synthese des Pflanzenschutzmittels Trifluralin.[4]
Biologische Bedeutung
Chloralin kann die Vermehrung von Parasiten wie Plasmodium falciparum oder Leishmanien hemmen. Es wird vermutet, dass die antiparasitäre Wirkung von Trifluralin auf Chloralin-Verunreinigungen beruht.[4]
Einzelnachweise
- ↑ a b c Datenblatt 4-Chloro-3,5-dinitrobenzotrifluoride, 99% bei Sigma-Aldrich, abgerufen am 3. November 2021 (PDF).
- ↑ A. R. Bucchi, A. Macri', N. Pellegrini, A. Pisani, C. Ricciardi: Acute oral toxicity in the rat of 3-nitro-4-chloro-alpha,alpha, alpha-trifluorotoluene (NCTT) and 3,5-dinitro-4-chloro-alpha,alpha, alpha-trifluorotoluene (DNCTT). In: Annali dell'Istituto Superiore Di Sanita. Band 19, Nr. 2–3, 1983, S. 351–354, PMID 6681224.
- ↑ Thomas A. Unger: Pesticide Synthesis Handbook. William Andrew, 1996, ISBN 0-8155-1853-6, S. 879 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b H L Callahan, Chase P. Kelley, Tércio Rodrigues Pereira, Max Grögl: Microtubule inhibitors: structure-activity analyses suggest rational models to identify potentially active compounds. In: Antimicrobial Agents and Chemotherapy. 1996, Band 40, Nummer 4, S. 947–952 doi:10.1128/aac.40.4.947.
