Chlorcyclohexan
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
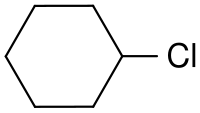
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Chlorcyclohexan | ||||||||||||||||||
| Andere Namen |
Cyclohexylchlorid | ||||||||||||||||||
| Summenformel | C6H11Cl | ||||||||||||||||||
| Kurzbeschreibung |
Flüssigkeit mit stechendem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 118,60 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,0 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
142 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
sehr schwer löslich in Wasser (0,4 g·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Brechungsindex |
1,462 (20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Chlorcyclohexan ist eine organische Verbindung. Es handelt sich um ein Derivat des Cyclohexans, bei dem ein Wasserstoffatom gegen Chlor ausgetauscht ist.
Herstellung
Chlorcyclohexan kann hergestellt werden, indem Cyclohexanol mit konzentrierter Salzsäure und wasserfreiem Calciumchlorid erhitzt wird.[2] Bei der Reaktion von Cyclohexen mit Chlorwasserstoff in Essigsäure entsteht Chlorcyclohexan sowie als Nebenprodukt Cyclohexylacetat. Dabei haben die Reaktionsbedingungen einen großen Einfluss auf das Produktverhältnis. Höhere Konzentrationen an Chlorwasserstoff führen zu einer besseren Ausbeute an Chlorcyclohexan, ebenso wie ein Zusatz von Tetramethylammoniumchlorid.[3]
Reaktionen
Durch Reaktion mit Magnesium kann Cyclohexylmagnesiumchlorid hergestellt werden.[2] Dies wird unter anderem zur Herstellung von Cyhexatin eingesetzt.[4] Mit Thioharnstoff bildet Chlorcyclohexan Einschlussverbindungen.[5]
Einzelnachweise
- ↑ a b c d e f g h i j Datenblatt Chlorcyclohexan, 99% bei Sigma-Aldrich, abgerufen am 8. Juni 2025 (PDF).
- ↑ a b CYCLOHEXYLCARBINOL. In: Organic Syntheses. Band 6, 1926, S. 22, doi:10.15227/orgsyn.006.0022.
- ↑ Robert C. Fahey, Michael W. Monahan, C. Allen McPherson: Hydrochlorination of cyclohexene in acetic acid. Kinetic and product studies. In: Journal of the American Chemical Society. Band 92, Nr. 9, Mai 1970, S. 2810–2815, doi:10.1021/ja00712a034.
- ↑ Thomas A. Unger: Pesticide Synthesis Handbook. William Andrew, 1996, ISBN 978-0-8155-1853-2 (google.de [abgerufen am 8. Juni 2025]).
- ↑ Kenneth D. M. Harris, John M. Thomas: Structural aspects of the chlorocyclohexane/thiourea inclusion system. In: Journal of the Chemical Society, Faraday Transactions. Band 86, Nr. 7, 1990, S. 1095, doi:10.1039/ft9908601095.

